
真题对于同学们复习的重要性想必同学们早就知晓了,那么本期唯寻就给大家挑选一些非常具有代表性的真题,通过唯寻的解析,希望能够帮助大家更好的复习,下面一起走进今天的IB化学HL试题精讲之Complex Ions单元。这一期为大家带来的是一道来自于2018年 May Chemistry HL paper 1的一道经典例题。

解题的第一步,是先读懂题目,抓住题根,进行审题——哪一个络离子(complex ion)的d轨道能量分离(d orbital splitting)最大?
从络离子(complex ion)以及d轨道能量分离(d orbital splitting)来看,这很明显是一道考察Periodicity中HL所学部分的Transition Metal和Complex ions的题目。这一题,我们可以直接从表格中的络离子颜色(Colour of complex)下手。因为络离子(complex ion)呈现的颜色的互补色(complementary colour)所具备的能量(energy)就是d轨道能量分离(d orbital splitting)后两个d轨道(d orbital)的能量差(energy difference)。
影响d轨道能量分离(d orbital splitting)的因素有很多,但其大小强弱最后都反应在了络离子(complex ion)的颜色上。表格中其他影响d轨道能量分离(d orbital splitting)的因素,如过渡金属的性质(nature of transition metal)、金属的氧化态(oxidation state of metal)或配体的身份(identity of the ligands)都会起到干扰作用。不能只凭这些因素中的一种或几种来判断d轨道能量分离(d orbital splitting)的大小。
虽然我们在paper 1的考试中不能借助data booklet-17. Colour wheel的帮助,但我们可以用“红橙黄绿蓝紫”这样的口诀来帮助我们回想起每个颜色的互补色。根据“能量(energy)越强的光,波长(wavelength)越短”这个定理,我们可以发现B所吸收的蓝光是4个选项中波长最短的,从而选出正确答案B。
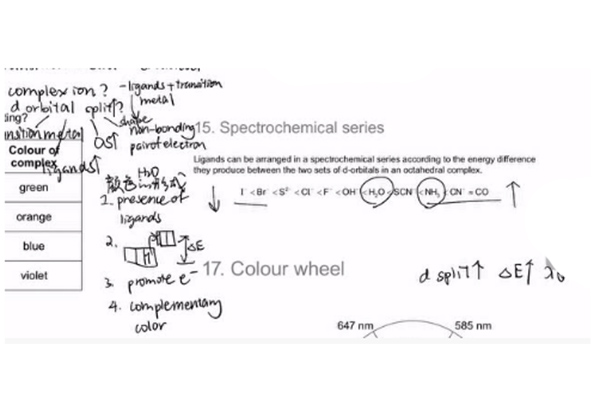
重难点解析:
1. 什么是transition metal?
It is an element that possesses an incomplete d sub level in one or more of its oxidation state.Zn(锌)不是过渡金属transition metal可以呈现不同的颜色
2. Complex ion的颜色是如何形成的?
配体(ligands)接近过渡金属(transition metal)后因为同性相斥(like charges repel),配体中的非建合电子对(non-bonding pair of electron)排斥过渡金属d轨道中的电子,d轨道分离,产生能量差异(energy difference),当白光(white light)照到络离子溶液上后,所具能量等于能级(energy level)能量差异的特定颜色的光被吸收,用来将电子推向更高的能级(promote electron to a higher energy level)。络离子溶液呈现被吸收的光的互补色(complementary colour)
3. 影响d orbital splitting的因素有哪些?
过渡金属的性质(nature of transition metal)、金属的氧化态(oxidation state)、配体的身份(identity of the ligands)、分子和离子的形状(shape of the molecule or ion)。
以上就是本期IB化学之旅给大家带来的真题讲解,如今化学在我们的生活中占据很重要的位置,化学也是英国很多大学专业的必修课程,所以同学们在平日的学习中一定要重视化成成绩哦。当然如果您有其他IB课程补习需求,欢迎您前来唯寻IB秋季班课程。

更多IB课程,尽在【干货 巧记IB化学酸碱盐溶解度规则和口诀】、【惊喜福利IB化学培训课程开班了 带你理清IB化学课程】。

学习有方法,成长看得见
筑梦牛剑/G5/常春藤
